PRESS RELEASE
2020年8月20日
株式会社EP綜合
富士通株式会社
EP綜合、富士通の医療機関向け治験ソリューション「tsClinical DDworks21/Trial Site」を採用
治験施設支援機関として初の採用、治験文書の電子化と効率化を推進
EPSホールディングス株式会社のグループ会社である株式会社EP綜合(注1、以下、EP綜合)は、富士通株式会社(注2、以下、富士通)が提供する「FUJITSU ライフサイエンスソリューション tsClinical DDworks21/Trial Site(ティーエスクリニカル ディーディーワークス21 トライアル サイト)」(以下、Trial Site)の導入を決定し、2021年2月から治験を実施する製薬企業や提携する医療機関向けに利用環境の提供を開始します。
「Trial Site」は、新薬開発を行う製薬企業と治験を実施する医療機関間でやり取りされる治験文書をクラウド上で共通管理することができるSaaS型ソリューションです。受託する試験数が少なく、システムを保有することが難しい医療機関は、EP綜合が保有する「Trial Site」を利用することで、個別にシステム導入のための費用を要することなく、治験文書の電子化と共有が可能となり、煩雑かつ膨大な文書作成や文書の授受に関する作成費用やトラベルコストの削減、保管に関するスペースや検索の効率化などが期待できます。
また本取り組みは、今般のコロナ禍における、文書授受時の接触機会の低減や、出勤抑制の際に書類印刷をどのように実現するかといった課題を解決します。「Trial Site」の活用による電子化は、製薬企業、医療機関双方の業務負荷を軽減させ、業務効率化やコスト削減に加え安全な業務遂行も可能となります。
EP綜合は、医療機関の治験業務支援サービスにおける電子化(保管を含む)に取り組むことで、治験環境の全体最適の実現に貢献します。富士通は、「Trial Site」の提供により、医療業界のデジタルトランスフォーメーションの加速を支援していきます。
背景
新薬開発のプロセスにおいて治験文書は、紙による運用が一般で、作成と印刷、ファイリング作業及び保管スペースの確保に加え、受け渡しを郵送や訪問で行う必要があり、効率化とコスト削減が喫緊の課題になっていました。そのため医療機関側、製薬企業側双方で電子化を進めて来ましたが、特に受託試験数の少ない医療機関側において、専用ソフトウェア導入に必要な多額の初期費用が課題となっています。
EP綜合は、業界トップの治験施設支援機関(Site Management Organization、以下、SMO)として、業界最大の提携医療機関数と幅広い疾患領域への対応力を有し、医療機関に対する支援を実施しています。今回、富士通が提供する医療機関向け治験ソリューション「Trial Site」を導入し、製薬企業と提携医療機関に利用環境を提供することにより、支援する医療機関における治験文書を電子化し、さらなる業務効率化を目指します。また、医療機関の電子化を推進することで、製薬企業のコスト削減にも貢献します。
「Trial Site」を利用した医療機関の治験業務支援サービスの概要
- 医療機関における治験文書の電子原本管理
医療機関内で作成される文書は、「Trial Site」のワークフロー機能を利用することで電子原本として保管されます。また、製薬企業が医療機関に文書を提出する際も、「Trial Site」を利用して電子的に交付を行い、医療機関側で受領されると電子原本として保管されます。保管のタイミングで、作成日時や試験名称などのメタ情報をもとに自動で適切なフォルダが作成されるため、確実なフォルダ管理や版数管理が可能となり、最新データへのアクセスが容易となります。また、治験文書における保管スペースの確保も不要となります。
- 効率的かつ確実なセントラルIRB(注3)の運営
これまで治験審査の依頼にあたっては、製薬企業と医療機関、IRB事務局が、紙を印刷し郵送などでやり取りをする必要がありました。また、IRB事務局は、文書のやりとりに加えてIRB委員へ配布する資料の準備や、審査資料の保管、審査結果を通知するための文書の作成といった業務が高い負荷となっていました。本サービスによって、治験審査の依頼はすべて「Trial Site」から電子的に行い、IRB事務局はシステムに集約された審査依頼と審査資料をもとに、委員への資料配布や審査結果の通知を電子的に行うことが可能になり、IRB事務局の業務品質およびスピードの向上を実現します。また審査を依頼する製薬企業にとっても、紙文書でのやり取りが電子に置き換わることで業務の負荷軽減につながるほか、印刷のために出社する必要もなくなります。
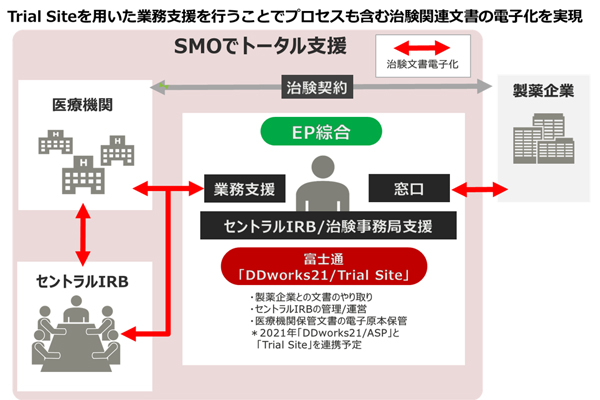
運用イメージ
拡大イメージ
今後について
EP綜合はセントラルIRBを足掛かりに富士通とさらなる連携を図り、将来的にはIRBを有する医療機関への「Trial Site」導入促進を目指します。治験環境の全体最適に向け、業務の負担軽減、品質およびスピードの向上を実現します。
富士通は、今後EP綜合との連携により「Trial Site」の医療機関への普及率を高め、製薬企業向けに提供する治験プロセス管理ソリューション「DDworks21/ASP(注4)」と連携することにより、治験フロー全体の電子化を推進し、さらに利便性の高いサービスの提供を目指します。
商標について
記載されている製品名などの固有名詞は、各社の商標または登録商標です。
以上
注釈
- 注1 株式会社EP綜合:
- 本社 東京都新宿区、代表取締役 社長執行役員 山本賢一。
- 注2 富士通株式会社:
- 本社 東京都港区、代表取締役社長 時田隆仁。
- 注3 セントラルIRB:
- Central IRB(Institutional Review Board)。 複数の医療機関から委託された審査を一括して行う特定の医療機関の病院内治験審査委員会。
- 注4 DDworks21/ASP:
- 富士通の製薬企業向け治験プロセス管理ソリューション。1997年に提供を開始し、84社のお客様に提供中(2020年7月現在)。
関連リンク
本件に関するお問い合わせ
株式会社EP綜合
管理センター 総務部
![]() 03-4218-3500
03-4218-3500
富士通コンタクトライン(総合窓口)
![]() 0120-933-200
0120-933-200
受付時間: 9時~17時30分(土曜日・日曜日・祝日・当社指定の休業日を除く)
プレスリリースに記載された製品の価格、仕様、サービス内容、お問い合わせ先などは、発表日現在のものです。その後予告なしに変更されることがあります。あらかじめご了承ください。