- > プレスリリース >
PRESS RELEASE (サービス)
2006-0079
2006年5月12日
富士通株式会社
「医薬品開発業務ソリューション」を刷新
~グローバルなコンプライアンス対応を支援する新コンセプトを確立~
当社はこのほど、医薬品開発におけるグローバルなコンプライアンス対応を体系化したコンセプトを新たに確立し、従来より提供してきた「医薬品開発業務ソリューション」を刷新しました。さらに、今回、本ソリューションを強化する4つのソフトウェア「e-Clinical RESERVOIR(イー クリニカル リザーバ)」「e-Clinical TICTAC(イー クリニカル チックタック)」「e-ECM PArcRoom(イー イーシーエム パークルーム)」「e-Clinical データ統合基盤」を開発し、本日より順次、販売を開始します。
これにより、グローバルな電子記録・電子署名に関する規制や医薬品の安全性に関する基準などに準拠したかたちで、新薬の開発期間のさらなる短縮と開発費用回収の加速化を支援します。
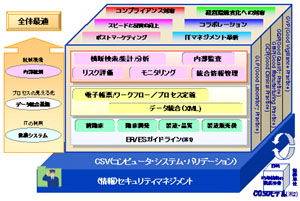 <<「医薬品開発業務ソリューション」の新コンセプト>> |
| 拡大イメージ |
製薬企業の研究開発投資が年々増加するなか、グローバルな新薬開発競争に勝ち抜くためには、開発のさらなるスピードアップや効率化が求められます。
特に日本における新薬開発は、欧米と比較して創薬研究力は高く評価される一方、治験での症例報告書(注1) など、医薬品開発プロセスの電子化の遅れから開発期間の長期化・開発費の増大が生じるケースが散見されます。また、近年、電子記録・電子署名に関する規制(注2)をはじめとするグローバルなコンプライアンスへの対応や、金融商品取引法で義務付けられる内部統制に対応すべく開発プロセスの透明性確保も求められるようになっています。
これらの課題に対し、当社は、医薬品開発におけるグローバルなコプライアンス対応を体系化したコンセプトを新たに確立し、これまで提供してきた「医薬品開発業務ソリューション」を刷新しました。このコンセプトは、米国の「21 CFR Part11」などの電子記録・電子署名に関する規制や、医薬品開発での非臨床試験・臨床試験・製造販売の実施に関する国際基準に準拠し、リスクマネジメントや情報漏洩対策などトータルな情報セキュリティを実現します。さらに、「業務システム」「データ統合基盤」「内部統制」の3層から構成されており、お客様の目的やニーズに応じて段階的なソリューションの適用が可能です。
また、SOA(注3)をはじめとする最新のITを活用することにより、社内に分散していた医薬品開発情報を統合し、業務プロセスの「見える化」を可能にすることで、内部統制をより確実にする4つのソフトウェアを新たに提供します。これらは治験の進捗管理や医薬品の安全性情報の傾向分析など経営判断に活用できます。
- 「e-Clinical RESERVOIR」(情報の統合と多面的活用)
日本のみならず海外での副作用や症例データなどの医薬品開発情報に関して、さまざまな切り口で横断的な検索・集計を可能にし、経営的観点から開発マネジメントを支援します。
- 「e-Clinical TICTAC」(治験業務進捗管理)
治験の症例・Visit(注4)ごとの進捗把握・監視により、治験プロセスの可視化、SOP(標準業務手順)に基づくコンプライアンス対応を実現します。
- 「e-ECM PArcRoom」(資料管理)
製薬業で使用されるさまざまな紙の資料、イメージデータ、電子ドキュメントとその資料情報を安全に管理・活用することが可能になります。
- 「e-Clinicalデータ統合基盤」 (医薬品開発の見える化)
SOAの考え方に基づく新たな統合基盤で、開発部門ごとに導入された業務システムから内部統制に必要な情報、ドキュメントを取り出し、経営管理に活用することが可能になります。
当社は、医薬品開発業務支援システム分野で、国内トップクラスの実績をあげています。また、医療・ライフサイエンス・製薬分野の業務支援システムの連携・融合に取り組んでおり、今後とも医療機関とのデータ連携や、先進ITを活用した個の医療を意識した治験などを支援してまいります。
なお、本ソリューションは、5月17日~19日、東京ビッグサイトにて開催される「製薬ITソリューションEXPO」に出展する予定です。
新製品の販売価格、および出荷時期
| 製品名 | 販売価格(税別) | 出荷時期 |
|---|---|---|
| e-Clinical RESERVOIR | 1,000万円より | 12月初旬 |
| e-Clinical TICTAC | 700万円より | 5月末 |
| e-ECM PArcRoom | 500万円より | 5月末 |
| e-Clinical データ統合基盤 | 個別見積 | 5月末 |
販売目標
今後3年間で売上100億円(「医薬品開発業務ソリューション」全体)
本ソリューションの特長
- お客様の業務情報管理レベルに応じた段階的導入が可能
以下の3つのレイヤーから構成され、お客様の目的やニーズに応じて、段階的導入が可能です。
- 情報セキュリティをベースとしたマネジメント基盤
リスクマネジメントや情報漏洩対策などトータルな情報セキュリティをベースとして製品・サービスを体系化しています。このため、外部委託やグローバル展開が進む医薬品開発において、ますます重要となるコンプライアンス対応が可能になります。
商標について
記載されている製品名などの固有名詞は、各社の商標または登録商標です。
以上
注釈
- 注1 症例報告書:
- 治験を実施した被験者に関する全ての情報を記載した書類。書くべき情報は、治験実施計画書において規定され、治験依頼者(製薬会社など)に報告される。「CRF (Case Report Form)」ともいわれる。
- 注2 電子記録・電子署名に関する規制:
- コンピュータシステムを利用する際に、紙ベースとの同等性を確保するための電子記録(Electronic Records)/電子署名(Electronic Signatures)に関する規制。米国FDA(米国食品医薬品局) の「21 CFR Part11」や、日本で2005年4月に厚生労働省から出された局長通知「医薬品等の承認又は許可に係る申請等における電磁的記録及び電子署名の利用について」(ER/ESガイドライン)が相当する。
- 注3 SOA:
- Service Oriented Architecture(サービス指向アーキテクチャー)。情報システム全体を サービスの集まりとしてとらえ、ハードウェアやOS・言語に依存せず、共通インターフェースを通じ、自由に連携・利用できるシステム構造を規定するソフトウェアアーキテクチャー。
- 注4 Visit:
- 被験者が来院するごとに結果を報告する症例報告書の形態。1つの冊子に最後にまとめて結果を報告する「冊子型」と被験者が来院するごとに結果を報告する「Visit型(分冊型)」 の2種類に大別される。
- 注5 GLP、GCP、GMP、GQP、GVP:
- GLP (Good Laboratory Practice) :医薬品の安全性に関する非臨床試験の実施の基準。
GCP(Good Clinical Practice) :医薬品の臨床試験の実施の基準。
GMP(Good Manufacturing Practice) :医薬品の製造管理及び品質管理に関する基準。
GQP(Good Quality Practice) :医薬品の製造販売後の品質保証に関する基準。
GVP (Good Vigilance Practice) :医薬品の製造販売後の安全管理に関する基準。 - 注6 CSV(Computer System Validation):
- 医薬品開発に関するコンピュータシステム構築において、一貫したシステム機能だけでなく、ユーザーニーズへの適合性や品質・セキュリティなどに対する厳格なテストを実施するとともに、証拠書類を基にした妥当性を検証すること。CSVは日本、米国、欧州など各国における要求事項になっている。
関連リンク
本件に関するお問い合わせ
ヘルスケアソリューション事業本部 ライフサイエンスシステム事業部 製薬R&Dソリューションセンター
電話: 03-6424-6215(直通)
E-mail: lssd-newsrelease@ml.css.fujitsu.com
プレスリリースに記載された製品の価格、仕様、サービス内容、お問い合わせ先などは、発表日現在のものです。その後予告なしに変更されることがあります。あらかじめご了承ください。
